El Futuro Es Ahora para la Anemia de Células Falciforme
Hay un dicho que dice que la ciencia parece magia si no se entiende lo que la hace funcionar.
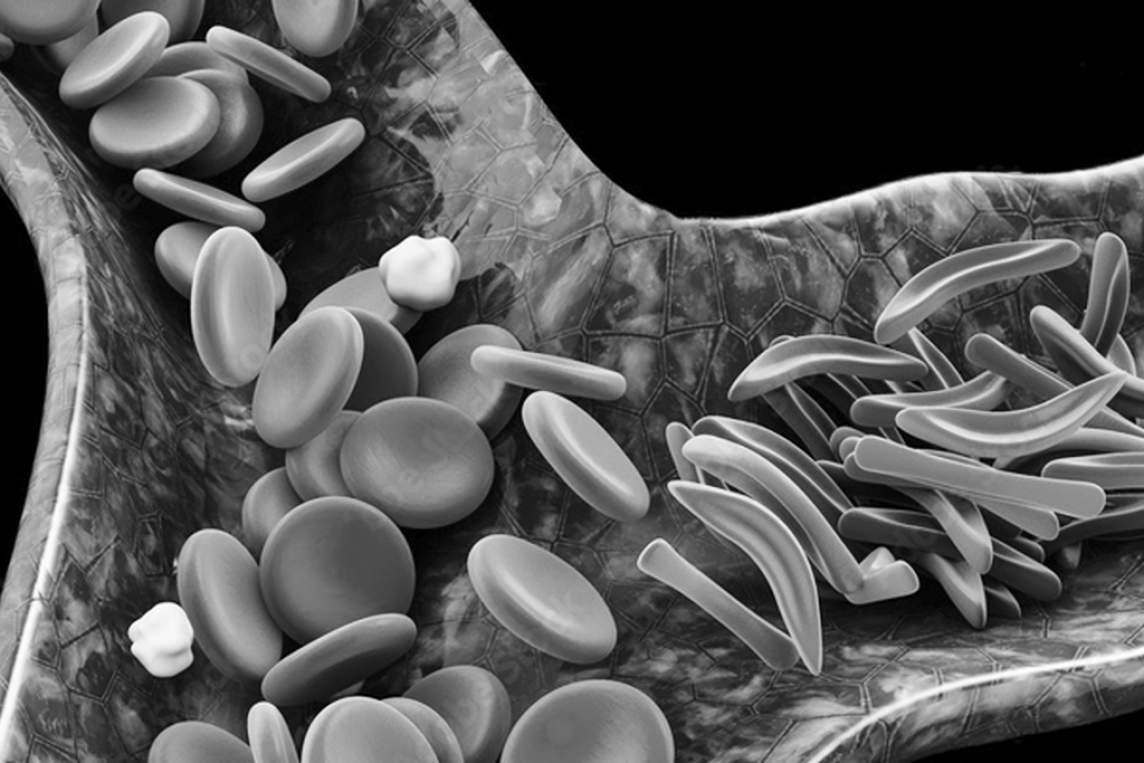
Esto es especialmente cierto en lo que respecta a la última terapia para la anemia de células falciforme (anemia drepanocítica), un trastorno que se observa en personas de ascendencia africana y siciliana. La enfermedad es causada por una anomalía en los glóbulos rojos que hace que la célula adquiera forma falciforme. La consecuencia de la falciformidad es la aglutinación de células y, a continuación, el bloqueo de los vasos sanguíneos pequeños. Los síntomas incluyen dolor, anemia, infecciones, problemas de crecimiento, apoplejía y varias complicaciones potencialmente mortales. Es de imaginar que todos los que padecen anemia de células falciforme o que han conocido a alguien con esta enfermedad han estado esperando con impaciencia mejores tratamientos. Hace años, le pregunté a un hematólogo especializado en anemia de células falciforme por qué no podemos hacer trasplantes de médula ósea. La respuesta fue que en ese momento las complicaciones podrían superar las posibles mejoras. Sin embargo, nuestra incapacidad para prevenir la drepanocitosis ha llevado a los científicos a seguir pensando en mejores formas de realizar un trasplante.
Los glóbulos rojos contienen una proteína especializada llamada hemoglobina, que es responsable de transportar oxígeno. Cuando hay mucho oxígeno, la hemoglobina lo retiene firmemente. Cuando los glóbulos rojos se mueven a áreas con poco oxígeno, la forma de la hemoglobina cambia y el oxígeno se libera. Esta maravillosa hemoglobina está compuesta de aminoácidos, y un error en un solo aminoácido en particular provocará la drepanocitosis. Si está familiarizado con la genética, puede preguntarse por qué este defecto en el código genético no ha desaparecido, ya que la enfermedad es tan incapacitante. Algunas personas pensaban que las personas originales con drepanocitosis en África tenían menos probabilidades de contraer malaria y, por lo tanto, sobrevivieron para transmitir la enfermedad a la siguiente generación, pero por alguna razón, el problema todavía está con nosotros.
En los últimos años, se ha desarrollado una nueva ciencia en la que los científicos pueden producir productos biológicos especiales para producir una tecnología llamada CRISPR; las moléculas especiales entran en las células y realizan ajustes en el ADN dentro del núcleo. El mecanismo exacto queda fuera del alcance de este artículo y no estoy seguro de poder explicarlo en unos pocos párrafos. Por lo tanto, supongo que para mí esta tecnología CRISPR es más magia que ciencia, pero es una parte importante del nuevo tratamiento para la anemia de células falciforme.
El primer paso del nuevo tratamiento es recolectar células especiales llamadas células madre que viven en la médula ósea y producen glóbulos rojos. Luego, las células madre se tratan con la tecnología CRISPR para corregir el defecto. Cuando las células madre tratadas se colocan nuevamente en la médula ósea, producen glóbulos rojos normales. Menos células falciformes y más células normales significan menos síntomas y menos complicaciones. Es como un trasplante de médula ósea, pero sin las complicaciones y los poderosos medicamentos antirrechazo.
Quizás se pregunte si esta terapia se aplicará a otros trastornos genéticos, y la respuesta es sí. Este tratamiento no es apropiado para todas las enfermedades genéticas, pero puede estar seguro de que los investigadores están trabajando febrilmente para aplicar esta técnica a muchos de los trastornos que podrían responder a la tecnología CRISPR.
El Dr. Robert B. Golenbock está actualmente jubilado. Ha atendido a niños en el área de Danbury durante 43 años, incluso en el Centro de Medicina Pediátrica. El CPM está ubicado en 107 Newtown Rd, #1D, Danbury, CT, 06810. Para más información, llame al (203) 790-0822 o visite https://centerforpediatricmedct.com.







